
藤原 裕展(ふじわら・ひろのぶ)
理化学研究所 生命機能科学研究センター
細胞外環境研究チーム チームリーダー
1998年京都薬科大学薬学部卒業。2003年大阪大学大学院理学研究科博士課程修了。理学博士。03年〜06年科学技術振興機構ERATO関口細胞外環境プロジェクト研究員、06年~07年大阪大学蛋白質研究所関口清俊研究室研究員。07年~12年英国がん研究所ケンブリッジ研究所フィオナ・ワット研究室研究員。12年理化学研究所発生・再生科学総合研究センター・チームリーダー。その後、組織改変等を経て18年より現職。

森田 梨津子(もりた・りつこ)
研究員
2005年東京理科大学卒業。2010年同大学基礎工学研究科博士課程修了。工学博士。13年理化学研究所発生・再生科学総合研究センター研究員。その後、組織改変等を経て現職。20年第13回資生堂女性研究者サイエンスグラント受賞。
ショートムービーで見る研究のあらまし
INDEX
毛包は生涯にわたって周期的に再生を繰り返す
夏になると、Tシャツやタンクトップに短パンということも多い。そんなとき、人間は哺乳類だなぁとつくづく思う。犬やサルなど他の哺乳類と比べると体毛は退化して薄くなってはいるものの、むき出しになった手足が毛におおわれていることがよくわかるからだ。
この体毛や毛髪は身体の保護や体温の調節など重要な役割を果たしており、人間のからだの中で皮膚とならんで再生能力が高いことで知られている。
毛が生涯にわたって産生されるのは、皮膚内に陥入して毛根を包んでいる「毛包」と呼ばれる皮膚付属の器官に存在する毛包幹細胞が、新たな細胞を生み出し続けるからだが、では発生の段階で毛包がどのように形成され、毛包幹細胞が分化していくのか、詳細なメカニズムはこれまで解明されていなかったという。
今年6月、理化学研究所生命機能科学研究センター(BDR)の研究グループが、毛包が形づくられる過程を詳細に調べ、毛包幹細胞の発生起源を明らかにした論文が「Nature」オンライン版に掲載され、そのニュースが世界を飛び交った。いったいどんな手法で取り組んだのか? にわかに興味を持って、神戸市にある理研BDRに伺った。詳しく解説してくださったのは、この論文の筆頭著者である研究員の森田梨津子先生と、チームリーダーの藤原裕展先生だ。
そもそも毛はどのように生え替わるのだろう? 森田先生がていねいに教えてくれた。
「毛包は、表皮が漏斗状にくぼんだ構造をしていて、くぼみの奥から毛が生えてきます。くぼみの中ほどの細胞が盛り上がった部分が、『バルジ』と呼ばれる領域で、ここに毛包を構成する細胞の供給源となる毛包幹細胞が集まっています。毛包が周期的に成長-退行-休止を繰り返す中で毛がつくり出されます。成長期に毛包幹細胞が爆発的に増殖することで生まれるのが毛母細胞。毛母細胞は毛根近くにあり、ここで活発に分裂・増殖し、毛を成長させます。退行期には、毛母細胞の細胞分裂が停止し、アポトーシスによって毛母が萎縮し、毛包はバルジの直下まで退縮していきます。休止期に入ると、毛包の活動はいったん休止。その後、毛乳頭がバルジの幹細胞を活性化させることで、新しい毛包が形成され、再び成長期へと進んでいくのです」
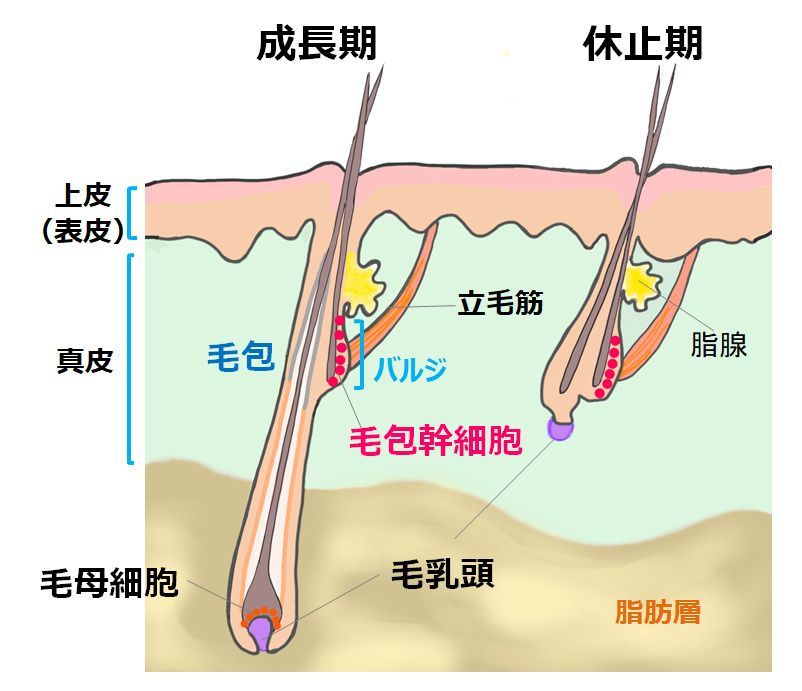
毛包の構造と毛周期
毛包幹細胞は、バルジと呼ばれる部分に存在して、毛包を構成する細胞をつくり出しているんだよ!
毛包幹細胞がバルジ領域に存在することが明らかになったのは、今から30年ほど前の1990年のこと。以来、毛包幹細胞についてはさかんに研究が行われてきたが、毛包幹細胞がどのように生まれてくるかの詳細は謎に包まれていた。
2016年にアメリカの研究グループが、マウスの成体にある毛包幹細胞のマーカー遺伝子の発現を手がかりに、毛包構造が形づくられはじめるごく初期に、基底上層細胞という種類の細胞が盛んに分裂を行って皮膚の深いところへと増殖し、毛包幹細胞になるという説を提唱し、これが定説として広く信じられるようになっていた。
「しかし、彼らが使ったマーカー遺伝子は、胎仔期においても発現しているものの、幅広い細胞で発現しているため、特定の細胞だけを区別することはできません。つまり、胎仔期の未成熟な上皮細胞の段階で、将来、毛包幹細胞になる細胞だけを標識できるマーカー遺伝子は見つかっていないのです。そこで私たちは、マーカー遺伝子に依存しない新しい手法で毛包幹細胞の起源を探る研究に取り組むことにしました」
毛包の発生過程をムービーで撮影し、時間を巻き戻して追跡
毛包幹細胞の成り立ちを解明するために森田先生と藤原先生が考えたのが、毛包の発生を1細胞ごとに追跡できる解像度でムービーを撮って、個々の細胞の時空間的な変化をライブイメージングによって探る方法と、1細胞ごとの遺伝子発現の変化を網羅的に解析する手法とを組み合わせること。
まず、細胞核で蛍光タンパク質を発現するよう遺伝子改変した受精後11.5日目のマウス胚から皮膚を採取し、生体外で培養する手法を確立。毛包の発生過程を、顕微鏡下で3~5日間にわたり、タイムラプスビデオで撮影した。この動画を逆再生して観察すると、成長して毛包を構成している細胞が発生初期にどの位置にいたのかが追跡できるというわけだ。
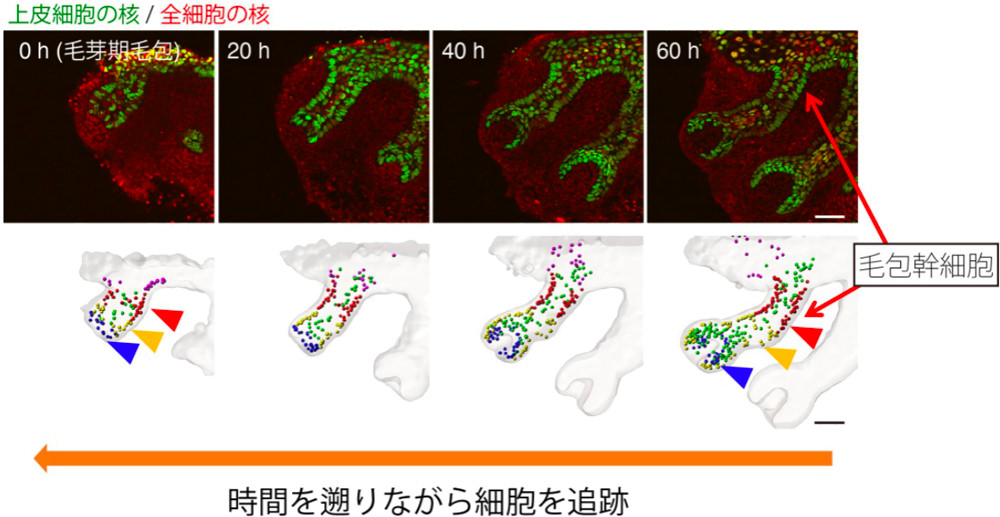
上:マウスの胎齢13日毛芽期毛包から、毛包が筒状の細長い形態を獲得する時期までの60時間をライブイメージング
下:上皮の各細胞を、時間を遡って追跡。将来幹細胞になる細胞(赤矢頭)は、毛芽期毛包の上部に存在し、他の細胞区画(黄、青)に移動しない。
スケールバーは100マイクロメートル(1μmは1,000分の1mm)。
Morita R, Sanzen N, Sasaki H, et al.
Tracing the origin of hair follicle stem cells.
Nature,June 2021 より
時間を遡って、ターゲットとなる細胞が
どこから発生したかを追跡したとはスゴイ!
「毛包は表皮の内側に埋もれるような形で存在していますし、あまり深部までだと光が届かない。ドンピシャで毛包が発生するところを顕微鏡で撮るために適切な場所をトリミングして、一連の発生過程をとらえた高解像度の動画を撮りきるまでは、けっこう苦労しましたね」
毛包は「プラコード」と呼ばれる平らな円盤状の原基から発生し、次第に皮膚の奥深くに向かって3次元の筒状の構造を形づくっていく。
時間を遡って細胞を追跡したところ、胎齢13日の筒状の形態形成が始まる発生初期の毛包ですでに細胞の運命が異なる区画に分かれていて、将来幹細胞になる細胞は上部の区画から誘導されることがわかった。
そして胎齢12日のプラコードの段階では、異なる系譜の細胞群が同心円状に組織化されて配置されており、将来、幹細胞になる細胞は、毛包プラコードの辺縁の基底層(図の赤矢頭)のリング状の部分から生まれることが明らかになった。
分析の結果、従来の定説で毛包幹細胞の起源とされていた基底上層細胞は、表皮内に散在しており、毛包発生にはほとんど寄与していないことも判明したという。
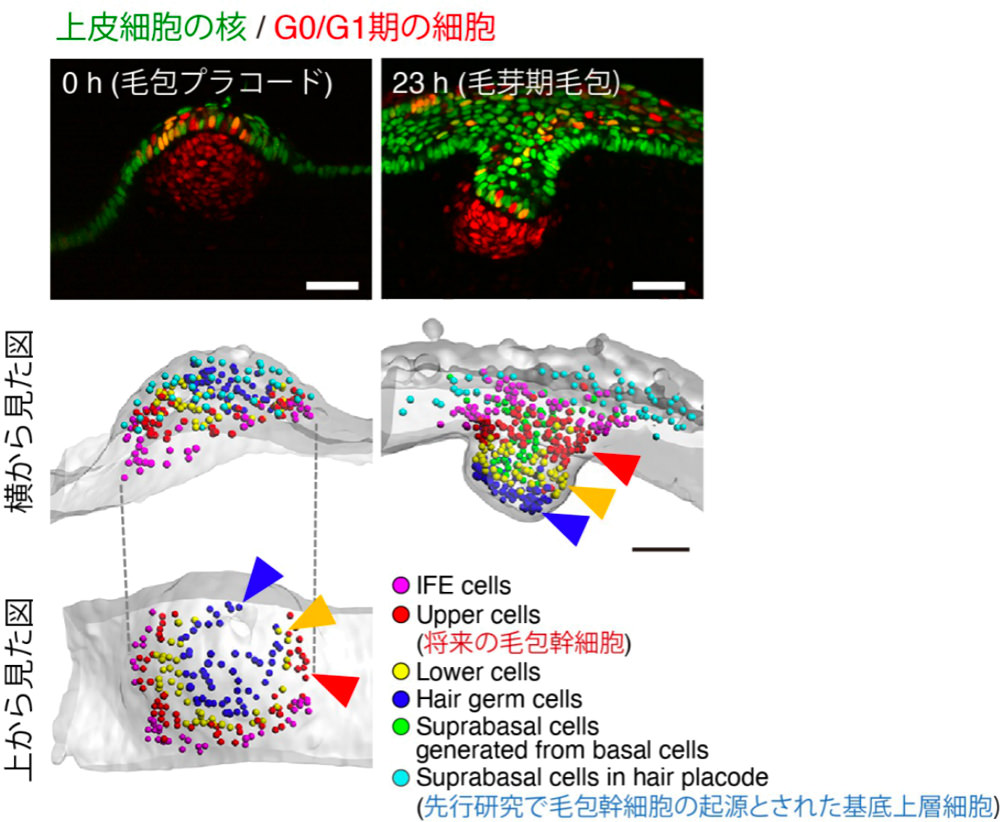
胎齢12日マウスの、プラコード期から毛芽期に至る毛包発生のライブイメージング(上)。毛芽期の各領域の細胞の動きを遡って追跡することで、プラコード期でのそれぞれの発生予定領域が分かる(下)。毛包プラコードには異なる上皮細胞系譜が同心円上に配置しており、将来幹細胞になる細胞は毛包プラコードの辺縁の基底層(赤矢頭)に存在した。定説で幹細胞の起源とされていた基底上層細胞(水色丸)は、毛芽期では表皮内に散在しており、毛包発生にほとんど寄与しなかった。
スケールバーは50μm。
Morita R, Sanzen N, Sasaki H, et al.
Tracing the origin of hair follicle stem cells.
Nature,June 2021 より
神戸から和光まで新幹線で移動して解析
続いて取り組んだのが、発生過程での毛包細胞の遺伝子発現の変化を解析すること。その手法が、「1細胞トランスクリプトーム解析」だ。
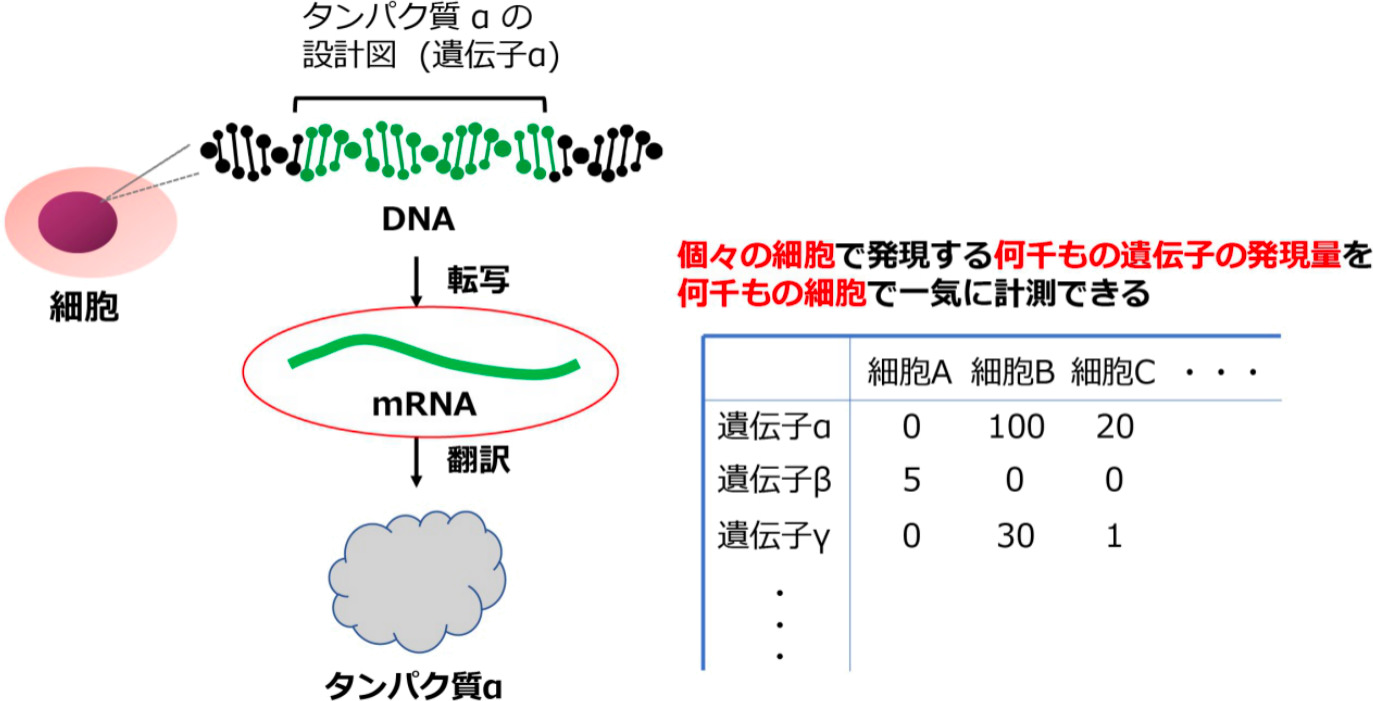
「トランスクリプトームとは、生体内の細胞に存在するメッセンジャーRNA(mRNA)の総体を意味します。私たちの細胞の核内には、遺伝情報としてDNAが格納されています。そのDNA上の遺伝子1個1個がタンパク質の設計図になっていて、DNAの情報がメッセンジャーRNA(mRNA)に転写され、タンパク質に翻訳されることでいろんな機能が発現していきます。個々の細胞で発現する何千もの遺伝子について、その種類や発現量のデータを、高速で自動処理できるDNAシーケンサーで一挙に計測しようというのが、1細胞トランスクリプトーム解析です」
発生過程の遺伝子変化のビッグデータを解析しようという研究だが、発生期の皮膚の下では、さまざまな発生段階の毛包が混在している。皮膚片を切り出すだけでは、さまざまな発生ステージ由来の毛包細胞の遺伝子情報がごっちゃになってしまい、精度の高いデータは得られない。
「トランスクリプトームの解析では、組織から細胞をバラしてしまうため、1個1個の細胞の位置情報が失われてしまいます。それを遺伝子発現の類似性などから再構築していかなくてはならないので、違う発生ステージの細胞が混ざっていると、精緻な解析ができなくなってしまうんです」
そこで、森田先生たちは、発生ステージの同じ毛包だけを取り出すため、特定の波長をあてると蛍光が緑から赤に変化するマウスをつくり、顕微鏡下で標識することで同時期の毛包の上皮細胞を高精度に単離する手法を開発した。
こうして得られた各発生ステージの細胞について、1細胞トランスクリプトームデータを得るために用いたのが、理研の二階堂愛博士の研究室が開発した「RamDA-seq」という1細胞完全長トータルRNAシーケンス法だ。これは、一つの細胞に含まれる10ピコグラム(1pgは1兆分の1グラム)という超微量のRNAの種類や量を、配列情報として網羅的に計測する手法で、従来の方法では解析できなかった、細胞分化や疾患、遺伝子発現の制御といった重要な生命現象に関与するRNAを含め、1つの細胞の中での多様なRNAのふるまいをまるごとライブラリー化できる。
「このRamDA-seqの解析ができる二階堂研は、当時埼玉県の和光市にあったんです。生きた組織での解析が必須なため、早朝の4時ごろに神戸の研究室でマウスの胎仔を解剖して解析用の組織を用意し、朝いちの新幹線に飛び乗って4時間半ぐらいかけて和光理研の研究室に行き、お昼すぎからソーティングする作業を行いました。7ステージぶんを解析したのですが、トライアルも含めて10回ぐらい神戸と和光とを行き来しましたね。二階堂研の林哲太郎さんに、ていねいにやり方を教えていただきました」
トランスクリプトームデータが取れたあとは、今度は、得られた遺伝子の発現パターン情報を統計的な手法で推定しなければならない。
「1細胞のRNAの配列情報を解析する『スーラ(SEURAT)』というソフトウエアをwebで見つけて、試行錯誤で解析を始めました。ほかのソフトウエアなども勉強しながら、自分なりのアレンジを加えて、ようやく狙い通りのデータがアウトプットできるようになっていきました」
こうして、トランスクリプトームデータから細胞の系譜と個々の細胞の組織内での時空間配置を再構築して分析を重ねた結果、ライブイメージングで得られた細胞系譜パターンと同様の同心円リング状の遺伝子発現パターンが存在すること、さらに、発生ステージの進行とともに、同心円の各リングで特徴的な複数の遺伝子が、同心円から筒状へと発現領域を変化させることが明らかになったという。
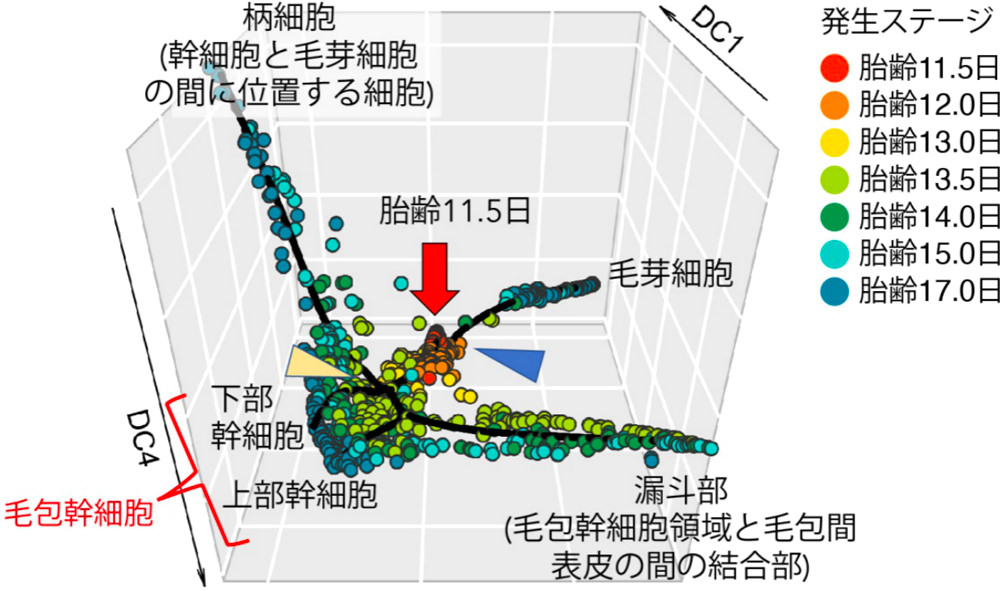
1細胞トランスクリプトームの再構築
各発生ステージの毛包上皮細胞の1細胞トランスクリプトームデータを用い、個々の細胞の遺伝子発現の特徴を三次元空間上の位置で表現したもの。
胎齢11.5日プレプラコード期(赤丸)を起点に、胎齢12日プラコード期(オレンジ丸)を経て、徐々に細胞運命が分岐して、それぞれの細胞系譜ごとに分化・成熟していく様子を捉えている。青矢頭は毛芽細胞の分岐点、黄矢頭は毛包幹細胞の分岐点を示す。
Morita R, Sanzen N, Sasaki H, et al.
Tracing the origin of hair follicle stem cells.
Nature,June 2021 より
「テレスコープモデル」と命名
ライブイメージングと1細胞トランスクリプトーム解析を通じて、毛包プラコード期には、異なる遺伝子発現のパターンを持ち、異なる細胞に分化する上皮細胞が同心円状に配置されていること、この2次元の円盤状の同心円パターンが体内側に陥入して、それぞれがタテ方向に伸びることによって、三次元的な筒状の毛包が形づくられることが明らかになった。
研究チームは、二次元のプラコード期から三次元の毛包の形ができていく様子が、まるで伸縮式の望遠鏡が伸びていくのとソックリというので、この形態形成の様式を「テレスコープモデル」と名づけた。
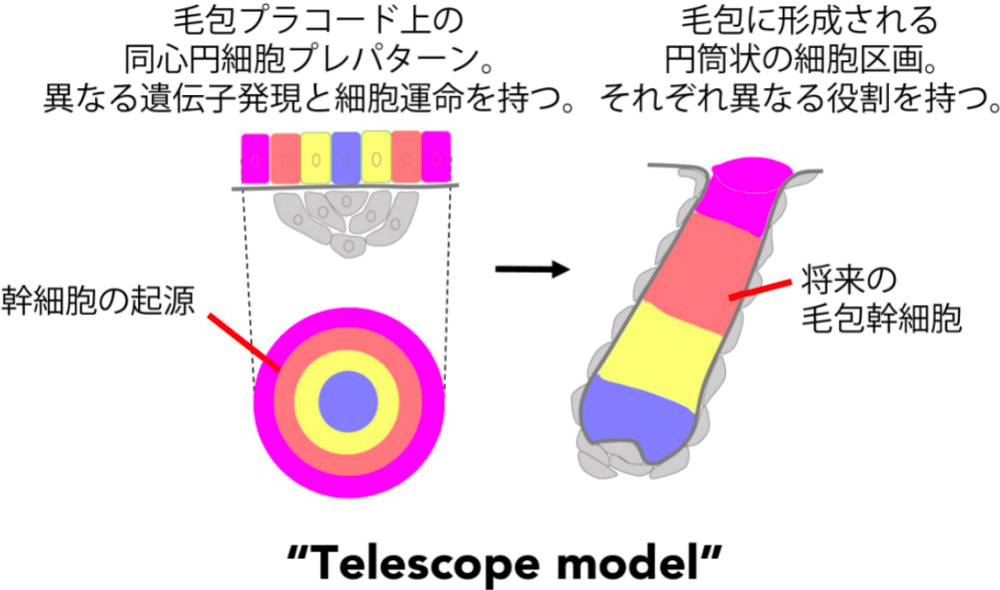
プラコードの同心円パターンは発生とともに体内側に陥入し、各領域が長軸方向に伸長することで、三次元的な筒状の区画が形成され毛包構造がつくられる。プラコードの同心円パターンの辺縁部(赤)が、将来の毛包幹細胞が誘導される領域。
2次元の円盤状から、三次元の筒状の毛包構造になる様子は、まるで望遠鏡が伸びるみたいだから「テレスコープモデル」と名づけたんだって。
「私たちは、このテレスコープモデルが、哺乳類の毛包にとどまらず、ほかの生物種の器官の発生過程でも存在しているのではないかと考えています。例えば、ショウジョウバエの肢の形成過程をみると、ハエの肢のもとになる未熟な二次元の上皮組織である肢原基は、同心円状に分化運命が定まった細胞が配置されていて、それぞれ肢の先端、中間、根元部分へと分化していきます。また毛包と同じようにプラコードから発生する乳腺や汗腺なども、同じようなテレスコープモデルで発生し、幹細胞が誘導される可能性があると見ています」
名前をつけようと提案したのは、チームリーダーの藤原先生だった。
「論文発表前に国内の学会でプレゼンテーションをしたとき、ほかの先生たちとディスカッションしたなかで、『まるで提灯のように伸びていくから、チョウチンモデルではどうか』というアドバイスをいただいたんですが、提灯では海外の研究者に伝わりませんからね。あれこれ考えた挙句、テレスコープモデルというのが一番しっくりくると考えました」(藤原先生)
新しい概念を提示する研究をめざせ
今回の研究の始まりは雑談からだったと、森田先生は語る。
「理研では毎年夏に大学生を対象にインターンシップをやっているのですが、うちの研究室で何をしようか検討したことがあるんです。そのとき私は、すでにマウスの胚を生体外で培養する系を確立していて、『ライブイメージングを動画で撮ってそれを巻き戻して追っていくと、幹細胞がどこから生まれるかが見えるんじゃないですか』みたいな思いつきを話したんですね。そのときは雑談止まりだったんですが、理研が持っている優れた技術と研究テーマを融合した研究に研究費がつくというグラント(助成金)があって、藤原先生がそのときのアイデアと1細胞トランスクリプトミクスを組み合わせるというアレンジをして応募したところ採択されて、2015年にプロジェクトがスタートしました」
そもそもなぜ森田先生は毛包幹細胞の研究に取り組むようになったのだろうか?
「学生のときは歯の再生についての研究をしていて、歯胚の原基をいったん完全に単一化した細胞にバラバラにして、それをもう一回人工的に組み合わせることによって歯胚の発生を再誘導するといった研究をしていました。その様子を顕微鏡で見ていて、器官の発生・再生の過程で、さまざまな細胞が常に適切な配置で誘導され複雑な器官の形をつくり上げていくのがすごくおもしろいなと思ったし、研究がとても楽しかった。ポスドクになろうと思ったときに、次のテーマを何にしようかと考えて、興味を持つようになったのが器官の再生を根幹で支えている毛包幹細胞でした」
一方の藤原先生が毛包幹細胞の研究に取り組み始めたのは、英国ケンブリッジがん研究所のフィオナ・ワット教授のラボでポスドクをしていた2007年のこと。それ以前から藤原先生は幹細胞に注目しており、特に、幹細胞の周囲の環境によって幹細胞の性質が維持されているのではないかと考え、その仮説を立証するために毛包幹細胞の研究を始めたのだという。
そして、毛包の幹細胞が「ネフロネクチン」と呼ばれるタンパク質を分泌し、幹細胞を包み込む特殊な環境をつくっていること、さらに毛包幹細胞がネフロネクチンを分泌するのは、毛包の隣にいる未成熟な細胞を立毛筋に成熟させ、毛包に接続して鳥肌(立毛)をつくれるようにするためだということを突き止めCELL誌に発表、帰国後の2012に理研でラボを立ち上げた。
このとき研究員に応募したのが、新しい研究室を探していた森田先生だ。
「毛包幹細胞とネフロネクチンについて論じた2011年の藤原先生の論文を読んで、こういう論文を書く人と一緒に仕事をしたいと思ったんです。細胞外マトリックスを介した幹細胞と周囲細胞の相互作用という新しい概念を提示していて、そういうことをめざす人なんだろうな、と感じました」
藤原先生は言う。
「サイエンスをやる上での大きなモチベーションは『誰も見ていない世界を見たい』ということです。新しいものの見方ができるのが何といっても楽しい。イギリスでの仕事も、最初は想定通りだったんですが、幹細胞が周囲の環境からシグナルを受けているだけでなく送り手にもなっていて、発生過程がそれまでわからなかった立毛筋に、新たな環境を与えていたという想定外の結果が出てきました。その考えを確かめさらに発展させるために実験を計画してデータを蓄積して論文をまとめました。このように、発見を通して自分の考えを表現できることがサイエンスとして一番わくわくするところです。
同じデータの解釈でも、そこには独自の視点があり、新しい見方を伝えられるかということが大切です。そのためには創造性や、『Think Different』という姿勢が大事。今回の研究は、毛包の発生と幹細胞の誘導についてまったく新しい視点を与えたこと、ほかの器官にも影響力のあるモデルを提示したことで、森田さんにとって代表的な仕事になると思います」
最後に、森田先生に今後さらに探究していきたいテーマについて伺った。
「幹細胞の起源が明らかになり、幹細胞が存在する場がどう形成されていくのかという謎に正しくアプローチできる状態になりました。そこを探究していきたい。また、テレスコープモデルの普遍性についても確認していきたいですね。さらに、毛包幹細胞の起源と発生過程が明らかになったので、こうした情報を生かして、将来的にはES細胞やiPS細胞から質の高い毛包幹細胞を効率よくつくり出すことにも道を開くはずです」
(2021年8月4日更新)

