ところで真下先生は、どのようなプロセスでゲノム編集を研究テーマとしたのだろう?
「例えば、私たちの身体の中にある2万個の遺伝子のたった1個のレプチンという遺伝子が変異を起こしただけで、極端な肥満になったりします。その1個の遺伝子を正常にしてやれば、病的な肥満を改善することができる。こうした例を知り、大学時代から遺伝子の勉強に取り組み始めました。遺伝子と病気の関係についてさらに探究したいと大学院に進み博士号を取得。パスツール研究所で西ナイルウイルスに感染したマウスで原因遺伝子を探る研究をし、帰国後は、疾患モデルラットをつくる研究を進めていました」
マウスでなくラットを対象としたのには理由がある。マウスとラットは似ているように思うかもしれないが、ラットはマウスより大きく、薬の安全性や効能を調べるにはマウスよりずっと適しているのだ。例えば血液がマウスの10倍もとれるので、いろいろな検査ができるという。
「なんとか遺伝子改変ラットをつくりたいと試行錯誤を続けていたとき、ZFN によるゲノム編集を知りました。これはすごい! 神の領域の研究ができるのではないかと興奮したことを今でも覚えています。そして、アメリカの企業が日本でもZFNを売り出そうとしているというニュースを知り、さっそくZFNを取り寄せて、ラットの受精卵に導入すると、なんとものの2か月間のうちに遺伝子ノックアウトラットをつくることができたのです。日本でのZFN利用の第1号となりました。ES細胞から遺伝子改変マウスをつくるには1年かかりますから、なんとすばらしい技術だろうと驚嘆したものです」
ただ、ZFNは先にふれたようにタンパク質をつくるのが技術的に難しく、効率も悪いなどの問題で限界もあった。その後TALENという植物病原菌由来の制限酵素も登場するうち、CRISPR- Cas9が登場。真下先生もCRISPRを使ったゲノム編集の研究を本格的に進めることになる。
「2014年には、ゲノム編集技術を使って遺伝子を修復する研究を行いました。例えば、メラニン色素合成を行う遺伝子が欠損したアルビノのラットと野生の茶色のラットとの差は、たった1塩基。野生型のある部分の『G』の塩基がアルビノでは『A』なのです。そこで、CRISPR- Cas9システムで『G』の塩基をノックインしたところ、アルビノのラットを野生型の茶色のラットにすることができました。ヒトの病気でもこのような1塩基だけが異なるという原因遺伝子はたくさんあるので、ゲノム編集によって病気の治療に役立てることができるはずです」
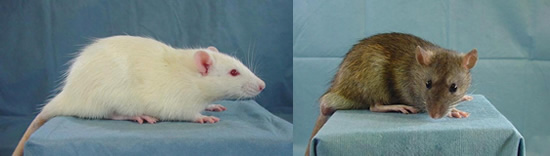
▲ アルビノのラット(左)、ゲノム編集で野生型ラットの毛色に(右)

▲ ゲノム編集によって、全身で緑色蛍光タンパク質を発現し、全身が緑色の蛍光を発するラット
ヒトの遺伝子ではサイズが大きいものも多い。そこで真下先生が2016年に挑戦したのは、1塩基よりもっと大きな塩基配列をノックインすることだった。
「私たちがトライしたのは、緑色に発色するGFP遺伝子をラットに注入することです。この写真をご覧ください。全身が緑色に光っているでしょう? ゲノム編集でつなぎ目のシール部分を工夫することによって、これまでの100倍の200キロベースのサイズの遺伝子を入れることに世界で初めて成功しました」
大きなサイズの塩基をゲノム編集で扱うことができれば、将来、ヒトの遺伝子の治療などに利用する際に応用できる。これは真下先生の研究の中でもとくに重要な研究で、特許を取得したという。

