頑強性に着目した「歩くナノ温度計」、「レシオ型ナノ温度計」、標的指向性に着目した「低分子蛍光温度計」を開発
鈴木先生がナノ温度計の開発をスタートしたのは2003年ごろのこと。当時、先生が在籍していた早稲田大学理工学研究科の石渡信一研究室に、ロシアからVadim Zeeb博士がやってきた。石渡研究室の持っていた、「タンパク質の繊維1本を温度計にする技術」を使って、細胞内部の温度を測りたいというのである。
「筋肉には、アクチンというタンパク質がつながった繊維があります。アクチン繊維が、ミオシン繊維という別のタンパク質繊維の上を滑るように移動することで、筋肉は収縮します。このアクチン繊維を精製し、温度が上がると暗くなる性質を持つ蛍光色素であらかじめ染めておきます。こうして、個々のくアクチン繊維を細いヒモ状の温度計にしようというのが、我々のラボの得意とする技術でした。Vadimとの共同研究の相手役に指名されたのが私だったのです」
最初に手がけたのは、ガラスのピペットの中に温度感受性のある蛍光色素を詰めておくというもの。ガラスにさえぎられるため、頑強性は問題ないし、熱伝導性も高いから感度も問題はなかったが、細胞内部に差し込むと細胞にダメージを与えてしまうので、細胞の外側からしか使えなかった。
そこで、次に温度感受性の高い蛍光色素を高分子で包み込んだナノ粒子をつくり、これを細胞内に取り込ませることにした。
「細胞が外界から物質を取り込む『エンドサイトーシス』という働きを利用するんです。粒子のサイズをある程度小さくして、球の外側をプラスにチャージした高分子で覆って細胞にふりかけると、細胞にくっついて中に入ってくれます。高分子が専門である早稲田大学の武岡真司研究室との共同研究だったのですが、最初は、まぜても球にならないとか、球が大きくなってしまうとか、色素が抜けてしまうなど、いろいろ苦労しましたが2012年に開発に成功。pHやイオン強度、粘性、タンパク質の濃度などの影響をシャットアウトして温度だけを計測していることが検証できました」
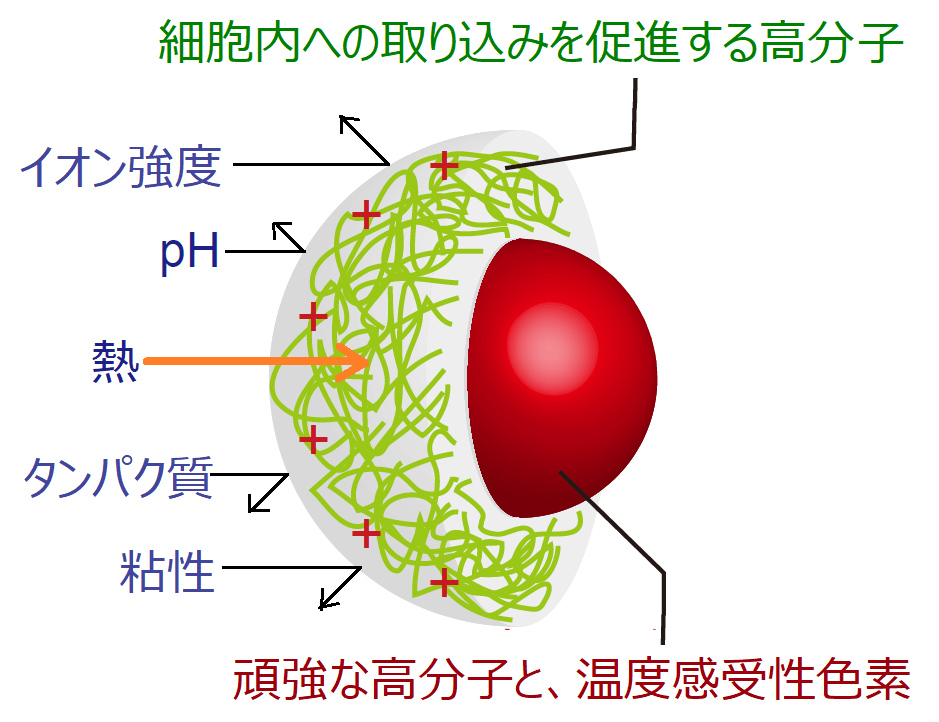
ナノ粒子型温度計のコンセプト。蛍光⾊素(⾚)を複数のポリマーで包むことで、他の環境因⼦(pHやイオン強度など)を遮断する。蛍光を発する中心核の粒径は約110 nm。
このナノ粒子型温度計は、標的指向性こそなかったものの、細胞内で「エンドソーム」という小さな袋状の細胞内小器官に取り込まれて、このエンドソームがタンパク質分子モーター(化学的エネルギーを力学的エネルギーに変換して仕事をする酵素)によって一方向に輸送されることがわかった。そして、細胞外部から瞬間的な熱パルスを与えると、分⼦モーターの酵素機能が素早く活性化され、加熱しているときだけ粒⼦の移動速度が上昇する現象が⾒られたという。
「言ってみれば、『細胞内を歩く温度計』です。粒⼦の位置と蛍光強度の時間変化を追った動画を画像解析することで、細胞内⼩器官の位置と温度がわかります。それまでにも細胞内の平均温度を測るタイプの温度計はあったのですが、動くタンパク質を蛍光ラベルすることによって、細胞の中で温度を測りながらタンパク質の働きも同時に見ることができる、世界初のナノ温度計となりました」
2014年にはこれを改良し、温度感受性の高い蛍光色素と感受性の低い蛍光色素を粒子内に封入し、2つの値の⽐率(レシオ)から温度をイメージングする技術も開発した。
「温度感受性の高い蛍光色素一つで測っていると、明るさの変化だけしか測れないので、今37℃なのか、それとも23℃なのかはわからないんです。また、細胞が動いたりすると明るさのシグナルはすぐに変わってしまう。それを補正するために、温度感受性の高いものと低いもの、2つの色素の測定値を割り算することで計測のブレをキャンセルすることにしました。これが『レシオ型ナノ温度計』で、細胞内の局所の温度や時間変動を1粒子で追えることが“売り”です」
「歩くナノ温度計」も「レシオ型ナノ温度計」も、標的指向性のほうには目をつぶって、感度と頑強性に着目して開発したものだった。では、標的指向性を追求した温度計へのチャレンジは、どのようなアプローチで進めたのだろう?
「細胞内の熱源は、筋肉であれば筋小胞体、褐色脂肪細胞ならミトコンドリアと言われています。そこで、低分子の蛍光色素をそのまま細胞内に取り込ませて、そうした小器官にターゲティングするような温度計をつくろうということで、シンガポール国⽴⼤学(当時)のYoung-Tae Chang教授らと共同研究を始めました。彼は蛍光色素のライブラリを持っています。その膨大なライブラリの中から、温度変化に応じて蛍光強度が⼤きく変化し、かつ、ねらった器官に集まる性質をもつ⾊素をスクリーニングしようというもの。かなりの力技が求められる研究ですが、Chang教授が得意とするところなんです」
まずスクリーニングに成功したのが、⼩胞体に集まる性質をもつ⾊素だ。測定の結果、温度上昇1℃あたり4%の蛍光強度の変化を伴う感度を有していて、細胞用の光温度センサーとして機能することがわかった。
しかも、遺伝子に組み込ませて導入するなどの面倒な手順は必要なく、細胞にふりかけるだけで、わずか数分間で、ターゲットとなる小胞体に特異的に集まり、温度分布を見ることができる。
「実際に、がん細胞の内部の熱源の直下にこの温度計を配置し、薬剤で刺激することでどのような温度勾配ができるかをリアルタイムで観察することにも成功しました」
がん細胞は正常細胞に比べて熱に弱いといわれる。鈴木先生らは細胞内の温度を測る技術とあわせて、細胞内を局所的に加熱する技術の開発と応用も進めている。これらを組み合わせることで、将来的には、⽬視ではわからない微⼩のがんを、顕微鏡下で実際の温度を測りながら死滅させるなどの応⽤が考えられるという。
その後2017年には、シンガポール国立大学のMichael Raghunath研究室、ハーバード大学のYu-Hua Tseng研究室らとの共同研究により、ヒト由来の褐色脂肪細胞が熱を生み出して温度が変化する様子を光学顕微鏡で観察することにも成功した。
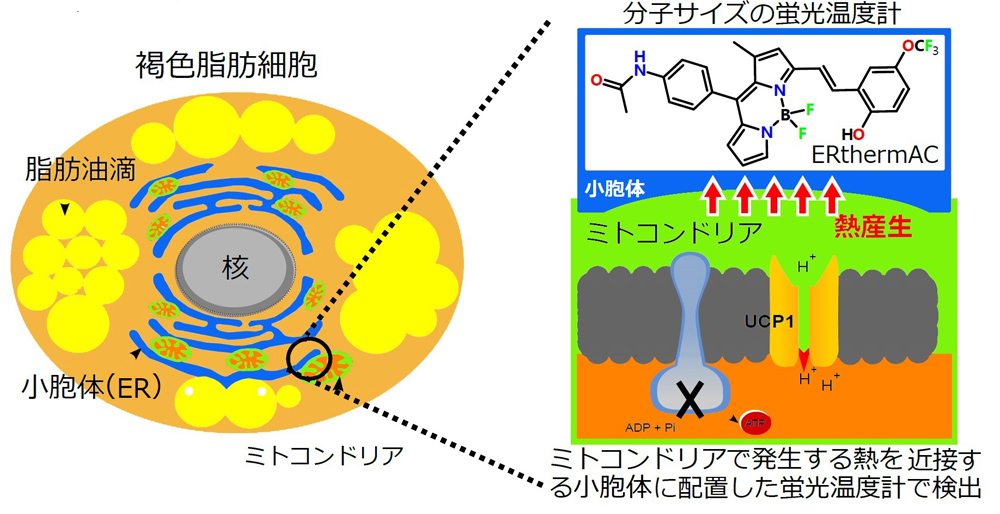
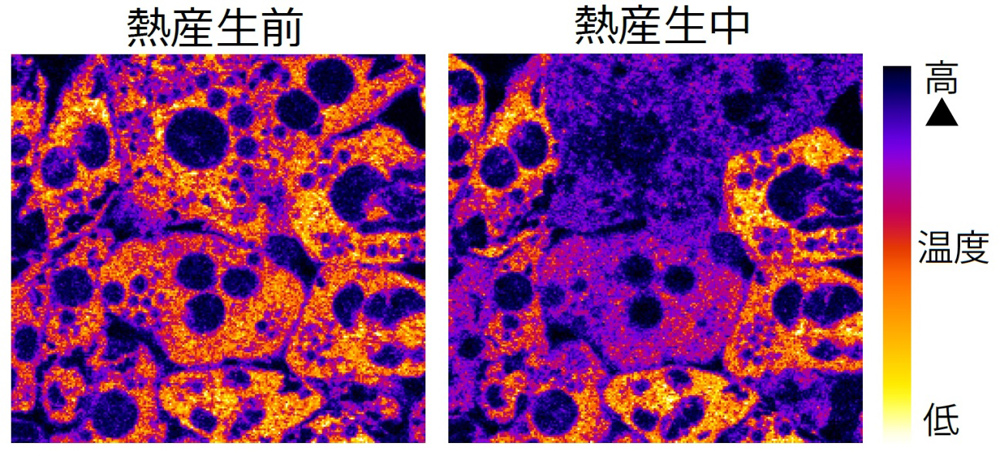
褐色脂肪細胞の熱産生を示した蛍光顕微鏡画像
Kriszt, et al. (Sci. Rep., 2017, 7, 1383)の一部を改変して転載。Copyright 2017 Nature Publishing Group