自分で考え自分で行動、これぞノビノビサイエンス
———NIHのラボではどんな研究をしましたか?
NIHでは分子薬理学の研究室(Yves Pommier教授)に所属しました。DNA修復の研究の延長で、抗がん剤の効きやすさ効きにくさを左右する因子の研究をしました。約30種類の抗がん剤と、いろんな遺伝子をノックアウトしたDT40細胞を約60種類使って、単純作業の実験をひたすら繰り返していました。作業は単調ですが、結果は薬剤や細胞ごとに違うわけで、結果が蓄積していくにつれ、いろいろな発見がありました。
———それはどんな発見ですか?
まず、PARP阻害剤という新規抗がん剤が、それまで考えられていた作用機序とは別の作用機序で抗がん作用を発揮していることを発見しました。PARP1というタンパク質は、傷ついたDNAを修復します。そのPARP1の機能を阻害することで、がん細胞に生じたDNAの傷が修復されないようにする、つまりがん細胞のDNAの傷を増やすことができると考えられていました。これはこれで正しいのですが、私は、PARP阻害剤にはさらに「PARPタンパク質をDNAに繋ぎ止めておく作用(PARPトラッピング作用と命名)」があることを発見したのです。2012年に発表したこの論文は、論文の引用数が検索できるGoogle Scholarで、現在引用数が1300を超えています。
思わぬ実験結果から、論理的に考察、実験し、Yves Pommier教授や同僚と毎日のように議論を重ね、真実に近づく興奮を味わいました。こんな風に、自分で考えて自分で行動して新しい生命現象を発見するという、研究者ならできて当たり前のことに、当時の私はようやく辿り着けたんですね。この論文を出したときに「研究者として生きていけるかもしれない」と思いました。
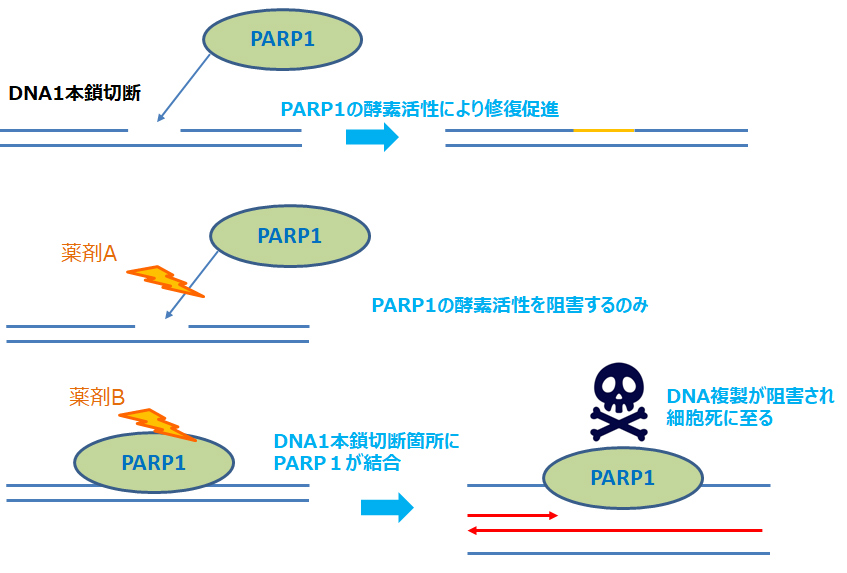
PARP1はDNAの傷(DNA一本鎖切断)の修復機能を持っている。PARP阻害剤は、PARP1のDNA修復機能を阻害するので、DNAの傷を増やして細胞死を導くと考えられていた。実際はPARP阻害剤を投与すると、PARP1は切断箇所のDNAに結合したまま離れなくなり(=DNAトラッピング)、DNAの複製を阻害することで細胞死を導く。つまりPARP阻害剤は、本来修復に働くPARP1酵素を毒に換える(=PARPポイズン作用)ことで、抗がん効果を発揮している。

2015年4月アメリカ癌学会で発表
帰国前の2018年9月、Yves Pommier教授とともに

ラボメンバーと(2018年9月)