脂質の観点から細胞膜構造を探る
———大学院を出たあと、研究をどのように展開していったのですか。
大切だけれども、まだ多くの人がその大切さに気づいていないような分野で、オリジナルの新しい研究をやろうと考えました。DNAマイクロアレイを用いた研究をしていたときに、上皮細胞にだけ高く発現する遺伝子には、細胞接着分子だけでなく、脂質代謝酵素があることに気づきました。ところが生化学では脂質の多様性を勉強するのに、細胞生物学ではタンパク質が主役で、脂質の役割についてはほとんど考えられていないのです。脂質は水にも溶けず小さいので解析が難しいこともあって、遺伝子がつくるタンパク質の機能ばかりに目が向いているんですね。教科書に載っている細胞膜のモデル図では、脂質分子は均一に描かれていますが、実際には細胞膜は膜タンパク質と同じくらい多様な脂質で構成されています。でもその役割や詳細な分布がわからないため詳しく描かれていない。昔の世界地図で、ヨーロッパや中東に比べて日本については情報がないため適当に描かれていたのと同じことです。
そこで、細胞膜にある数千種類にも及ぶ多様な脂質を解析して、脂質が細胞膜構造を形づくる上でどういう役割を果たしているのかを明らかにしたいと考えました。月田先生が形態学の観点から研究してきた細胞膜構造を脂質の観点から研究することで、新しいものが見えてくるのではないかと考えたのです。
———脂質から細胞膜構造を研究しようと考えて、どうされたのでしょう?
当時、脂質の可視化に着目する数少ない研究者の一人が、京都大学化学研究所の梅田眞郷(うめだ・まさと)先生でしたので、ポスドク*としてお世話になることにしました。梅田先生のもとで習得した脂質の実験手法をもとに、生化学や分析化学と細胞生物学をつなぐための新しい実験技術を確立しようと試行錯誤を続けました。2008年には准教授になり、2010年に先生とともに工学研究科の合成・生物化学専攻に移ったことで、工学と化学、生物学が融合した大学院で、学際的な視点でいろいろなアイデアを得ることができました。
*ポスドク:ポストドクトラルフェロー/リサーチャー(Postdoctoral Fellow/Researcher)の略。博士号取得後に大学や研究機関でつく研究職のこと。博士研究員ともいう。
———世界では、脂質の働きに着目した研究は行われているのですか?
例えば、ドイツの細胞生物学者、カイ・シモンズ(Kai Simons)は1997年に「脂質ラフト説」を提唱しています。細胞膜の主成分であるリン脂質に特定の脂質を混ぜると、親和性の高い脂質同士が集まって膜の中にラフト(筏)のように分かれます。細胞膜上の多様な脂質がそれぞれ独自のラフトを作り、さらに親和性のあるタンパク質を集めることで情報の伝達や物質の移動を行っているというのです。この現象は人工膜の実験では証明されていますが、細胞の中で同じことが起きているかどうかはまだ確かめられていません。
———脂質の働きを探るための手法にはどのようなものがあるのですか。
ウエルシュ菌のタンパク質由来の毒素がコレステロールに結合する性質を利用して、細胞内のコレステロールを可視化する技術が開発されています。
細胞膜の脂質組成を知るには、細胞膜だけを単離する必要があります。私はシリカ粒子を結合させることで細胞膜を物理的に単離する手法を開発し、これと質量分析とを組み合わせて、細胞膜を構成する脂質分子を明らかにすることに成功しました。
———脂質から細胞膜構造を探る研究が本格的にスタートしたわけですね。
海外も含めて細胞膜の研究が盛んになってきましたし、分析技術も進んで微量な脂質の組成解析も可能になっていますから、脂質の新たな機能や重要性も明らかになりつつあります。ただ、有機溶媒にしか溶けない脂質は扱いが難しく、タンパク質や核酸よりも実験のハードルが高いです。脂質の解析がもっと一般的な技術になれば、より多くの知見が集まるはずです。ある現象をタンパク質で説明できないときに、別のタンパク質の存在を考えると同時に脂質の関与も考えられるようになれば、細胞の世界はもっと鮮明に見えてくるでしょう。
———2013年に九州大学でご自分の研究室を持たれました。どんな研究をテーマに掲げたのですか。
今申し上げた、細胞膜構造の形成における脂質の役割を明らかにすることが一つ。また上皮細胞の異常によっておこるがんや線維症などの病態と脂質の関連についても探っています。
———がんと脂質との関係について教えてください。
さきほど、「スネイル」という遺伝子が上皮細胞に発現すると上皮細胞の細胞膜の接着構造が壊れて、がん細胞が移動できるようになり、浸潤・転移していくとお伝えしました。おそらく遺伝子が傷つくことで正常な細胞にスネイルが発現するようになるのですが、スネイルは転写因子で核の中に存在するので、抗体でやっつけるわけにはいかず治療法がないのです。先ほど述べましたように、上皮間葉転換の際には脂質を代謝する酵素の発現が変化します。細胞のがん化に伴って、脂質の組成が変化することが、がん細胞の振る舞いにどのような影響を与えるかについて、現在解析を進めています。
また、上皮細胞集団の中でがん細胞がどのように浸潤していくかも重要な問題です。ここで私たちが注目しているのが「ブレブ(Bleb)」という細胞膜構造です。ブレブは、細胞膜を支える骨格の一つであるアクチンというタンパク質がはずれると、その部分の膜が焼き餅のようにプウっと膨らんでできます。ブレブは細胞が分裂したり死んだりするときにできると言われていましたが、じつは最近になって、細胞はブレブを使って能動的に膜突起を出しながら移動していることがわかってきました。そしてがん細胞は、上皮細胞の下に存在する細胞外マトリックスと呼ばれるコラーゲンなどのタンパク質の網目の中をかいくぐるようにして動き回ります。どのようにブレブが形成されるのか、アクチンがどうしてついたり離れたりしてブレブが移動するのかのメカニズムがわかれば、がんの浸潤・転移の予防に役立つはずです。
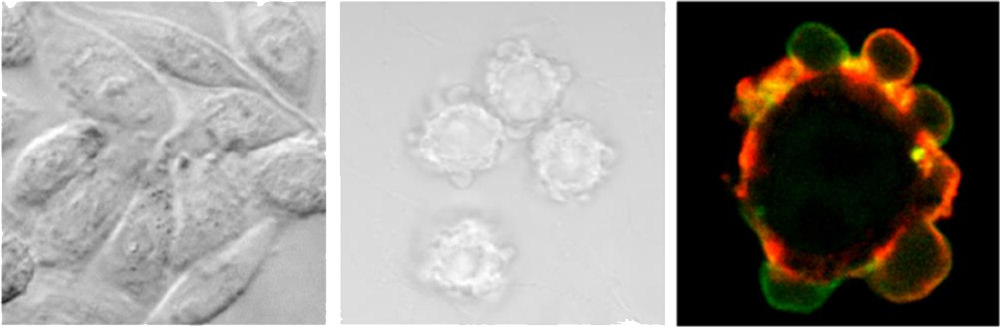
プラスチックの上で培養(左)、コラーゲンに埋め込んだ状態で培養(中)、ブレブが形成されているがん細胞(右)
2016年3月九州大学プレスリリース「癌細胞の浸潤や転移に関わる細胞運動の仕組みを解明」より
コラーゲン内でブレブが移動している様子
———なるほど。臨床にも役立つ可能性があるのですね。
医学部出身ですから、新しい治療の標的を見つけたいという思いもあります。遺伝子に着目したがん治療が進んでいるように、脂質に着目した新しい治療法ができればいいですよね。
タイトジャンクションが破綻すると、菌が侵入して皮膚炎や潰瘍性大腸炎などの病気を引き起こしますが、現在ある治療法はほとんどが、免疫応答を抑えたり、痒みを抑えるといった対症療法です。根本的な治療としては、タイトジャンクションのバリア機能を強くする方法を確立することが必要ですが、クローディンをたくさん発現すればタイトジャンクションのバリア機能が強くなるというわけでもないんですよ。最近、私たちは、上皮細胞には常にクローディンが大量に備蓄されていて、細胞がストレスにさらされると速やかにタイトジャンクションの形成を増強してストレスから上皮を守れるようにしていることがわかりました。ですから一つのタンパク質だけでなく、脂質も含めて、細胞膜構造の形成メカニズムの全体像を理解しなければなりません。
———研究をする上で、特に大事にしていることはありますか?
目の前にある情報の中で意識的、無意識的に省かれている要素をどれだけ想像できるかがとても大事です。例えば、教科書というものは疑念を抱かせないために、確実にわかっていることしか書きません。細胞接着分子の模式図でも2つの接着面しか描かれていませんが、実際には3つの細胞が接しているところがあるわけです。しかし、うまく説明できないので省いてしまう。脂質の多様性に関しても同様です。
だから教科書であっても、どういう根拠でここまで言い切っているのか、模式図で省略されている要素はないかと懐疑的に読んでみる。教科書に書かれていないところに大事なものがあるのではないかと思います。
———書かれていないことを見つけるには、どうしたらよいでしょう。
大切なことは「研究者の視力」を鍛えることです。これは月田先生も口を酸っぱくして仰っていました。道端に珍しい花が咲いていても、その花のことを知らなければ素通りしてしまいますね。それに気づく視力を鍛えるには、やはり学生時代に幅広く勉強することです。自分の専門のほかに、どれだけ関連する視点や知識を持っているかが生きてくる。そのためにも、いろいろなことに興味を持ってできるだけ幅広く学んでください。
私も出身は医学部ですが、ポスドクで入った化学研究所では化学系の研究者、その後は工学系の研究者とも接点がありました。異分野の先生と交流する中で多様な視点を持つことができたと思います。その意味では、異分野であっても自分の研究とは関係ないと決めつけないことも大切にしてください。
(2023年11月20日更新)