骨の強さを決めるメカニズム
———生物学的にはどんな研究をしたのでしょう。
プレート表面につける溝の形状で細胞の向きが決まる過程で、細胞の間で何が起こっているのか、そのメカニズムを生化学的に解明するのは私にしかできない役割だと気づきました。ノックアウトマウスを使って、骨の発生学的なプロセスを解明しながら材料との関係を調べていくことになりました。
———具体的にはどんなことを調べましたか。
たとえばマウスの場合、まれに破骨細胞がない個体がいます。破骨細胞がなくても骨芽細胞があれば骨は増えるから問題はなさそうですが、じつは破骨細胞がないマウスは結晶の向きがバラバラで骨折しやすいんです。
もしかしたら、破骨細胞と骨芽細胞が協力して結晶の向きを決めているのかもしれない。そう考えて、複数の細胞を同じ環境で培養する「共培養」の手法を応用した装置を作って調べてみました。破骨細胞と骨芽細胞をそれぞれ培養し、細胞に与えた刺激が双方に伝わるようにして、配向がどのように制御されているかDNA解析なども行って調べていったのです。破骨細胞は骨を吸収するときに酸を出して骨を溶かしますが、そのときに酸以外にもいろいろな物質を分泌しています。その働きを調べていくと、その中の特定の分子が、骨芽細胞に配向を揃える情報を伝えているとわかりました。だから、破骨細胞がないと結晶の向きがバラバラになっていたんです。
———骨芽細胞と破骨細胞が情報のやりとりをしていたんですね。
さらに、骨の奥には「オステオサイト」という力を感じるセンサーをもつ骨細胞があります。その働きも詳細はわかっていませんでした。そこでオステオサイトの働きを共培養で調べてみると、やはり骨芽細胞と情報伝達をして骨の配向を制御していること、そしてここには、「PGE2」という脂質分子が関わることがわかりました。
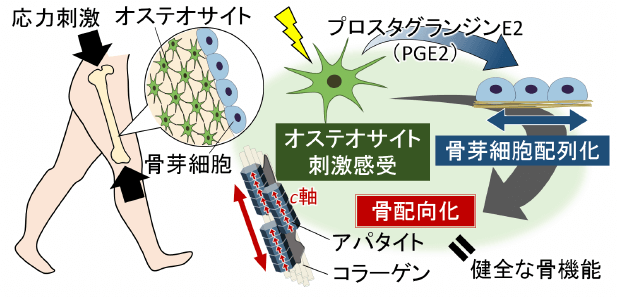
応力を感受するセンサー役をはたすオステオサイトは、PGE2を分泌し、骨芽細胞を一定の方向に配列し、配向化骨を形成する。
(2021年10月26日プレスリリースより)
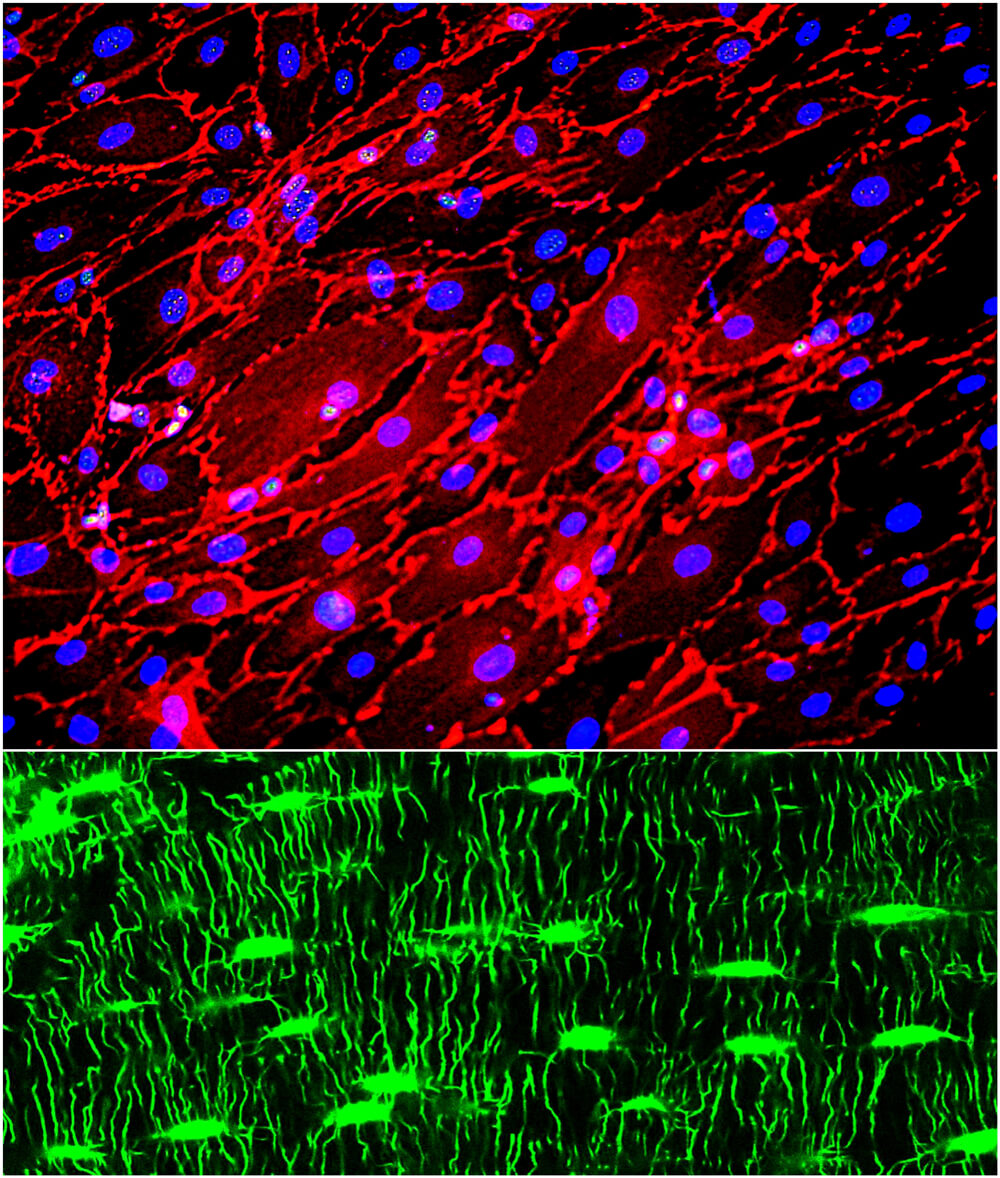
骨の働きを決める、骨芽細胞(上)とオステオサイト(下)。細胞への物理刺激は骨芽細胞の方向性をコントロールして、骨配向性を生み出す。
———そのほかの研究について教えてください。
骨の病気は数多くありますが、歩行などの日常生活にダイレクトにつながる器官なので、その治療や予防に役立つ研究をしたいとの思いから、骨の重要な疾患についても調べました。骨は骨髄に栄養が豊富にあるため、がんが転移しやすいんです。しかも、ある種のがんでは骨が異常に増えるため骨密度は上がるのに骨はもろくなる。そこで、がんの研究経験がある研究室の関田愛子(せきた・あいこ)さん(現 理化学研究所 研究員)と転移のしくみも調べました。すると思った通り、がん転移した骨は結晶の配向が大きく崩れていました。
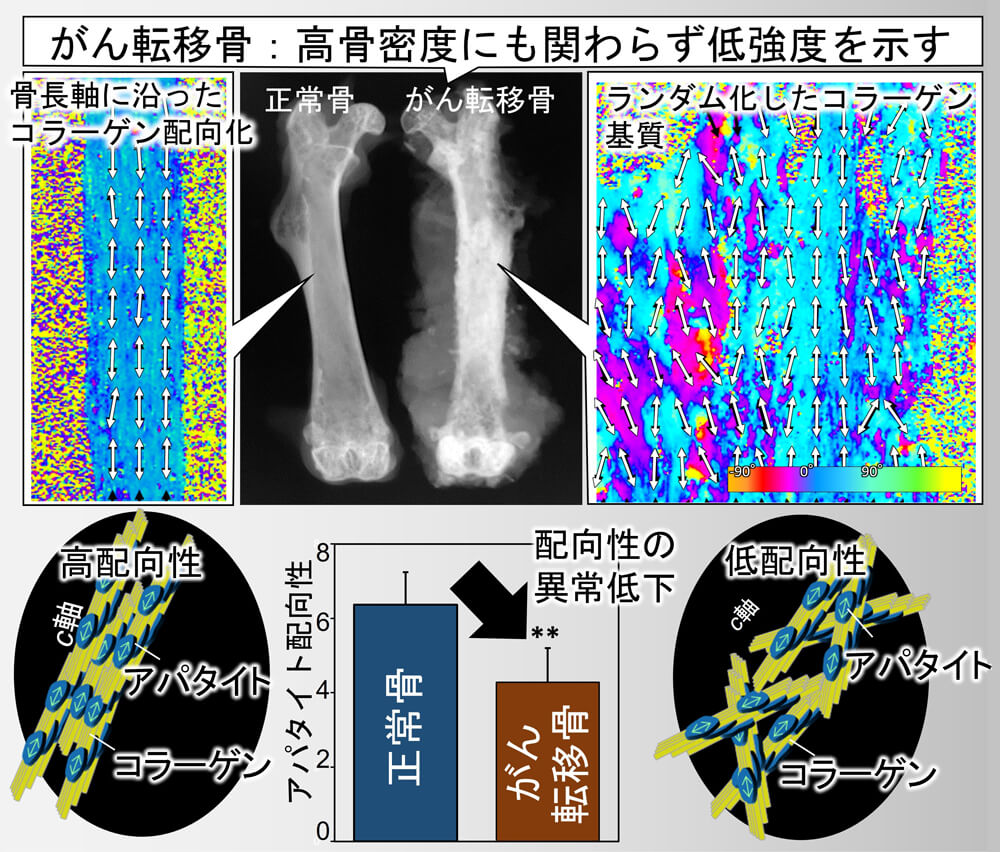
がんによる骨劣化の原因は、骨配向性の異常である。
———骨がもろくなるのは骨密度のせいじゃなかったんですか!
そうなんです。骨の強さというと「骨密度」が大事だといわれますが、むしろ配向性が非常に重要だとわかってきたのです。宇宙飛行士や寝たきりの方の骨が弱くなるのは「骨に力がかからないことで配向性が阻害される」のがおもな原因だったんですね。